Не забывайте о том, что после обработки поверхностей с использованием Permatex Rust Treatment, необходимо выдержать их в течение хотя бы суток перед нанесением краски или грунта. За этот период препарат полностью высохнет, что позволит избежать возможных химических реакций между материалами.
Чем защищать металл от коррозии Статья
Существует множество различных материалов, перечень которых может быть весьма обширным. Металлы занимают одну из ведущих позиций среди всех материалов, употребляемых в различных сферах и для самых разнообразных целей. Важно отметить, что металлов существует крайне много (если учитывать сплавы) и у каждого из них есть как достоинства, так и недостатки. Наиболее притягательным моментом, связанным с металлами, является их склонность к коррозии, которая со временем может уничтожить их. Процесс, о котором идет речь, мы обычно обозначаем термином «ржавение». В данной статье мы займемся детальным анализом причин коррозии, выясним, какие металлы наиболее подвержены этому процессу и, что наиболее важно, обсудим способы их защиты от ржавления. Если хотите сразу перейти к практической части, вы можете перейти прямо к третьему разделу нашего материала.
Мы не будем погружаться в сложные химические процессы, однако стоит отметить несколько основных аспектов и развеять распространенные мифы. Прежде всего отметим, что коррозия охватывает, в первую очередь, черные металлы, такие как сталь, чугун и железо. Многие считают, что цветные металлы не ржавеют, но это заблуждение. Действительно, цветные металлы, такие как медь и алюминий, также могут подвергаться разрушению. Однако они это делают очень медленно или только в определенных условиях. Например, в тех местах, где сталь может разрушиться за 50 лет, медь может сохраняться гораздо дольше. Более того, коррозия может быть вызвана не только контактом с водой, как обычно думают, существует множество других факторов, способствующих разрушению.
Любой вид коррозии возникает из-за определенных химических реакций, и в этих процессах могут взаимодействовать различные вещества. Некоторые металлы или сплавы активно ржавеют в водной среде, в то время как другим требуется контакт с воздухом или кислой средой, а третьи подвергаются разрушению в среде электролитов — это явление известно как электрохимическая коррозия. Но это лишь небольшая часть существующих механизмов, и, следовательно, для нас важным остается вопрос о том, как защитить металлы от коррозии в условиях, когда они подвергаются воздействию воды или кислорода.

Каждый металл обладает своими уникальными характеристиками. Например, у стали можно выделить несколько типов коррозионного поражения: это и поверхностная коррозия, и трещины, которые могут проникать вглубь материала, и другие формы повреждений. В любом случае, если металл подлежит коррозии, необходимо принять меры по его защите. Существует множество методов защиты, различающихся по стоимости и надежности. В некоторых случаях защитные меры совершенно отсутствуют, что и приводит к тому, что мы часто сталкиваемся с ржавыми металлическими изделиями. Это связано, прежде всего, с экономическими факторами.
Существует множество типов защиты от ржавчины (подробно об этом поговорим ниже). Они могут быть как базовыми (например, добавление различных ингибиторов), так и временными мерами (защитные покрытия). Второй вариант чаще всего оказывается более доступным, что объясняет его широкое применение. Именно поэтому возникает вопрос, как быстро и эффективно защитить металлические изделия от коррозии, особенно если защитный слой уже поврежден. Не стоит переживать, это не так сложно и дорого, важно лишь действовать оперативно и не медлить, пока ржавчина не проникнет слишком глубоко в металл.
Способы защиты от коррозии
Способы защиты можно классифицировать на две крупные категории: промышленные и бытовые. В рамках нашей статьи основной акцент будет сделан на бытовые способы, так как вероятнее всего, люди, использующие промышленные методы, не нуждаются в таких руководствах. Тем не менее, имеет смысл упомянуть и о них. К промышленным способам защиты от коррозии можно отнести следующие:
Пассивация металлов. В данном процессе металл, или его поверхность, переводится в состояние, которое препятствует возникновению коррозии (это состояние называется пассивным или неактивным). Эта процедура достигается в основном за счет использования легирующих добавок, таких как хром, никель и так далее. Например, в состав широко известной нержавеющей стали добавляется хром для повышения её коррозионной стойкости.
Нанесение защитных лакокрасочных покрытий, которые предотвращают контакт металла с окружающей средой. Это один из самых популярных методов, поскольку он является относительно дешевым и простым. Однако стоит помнить, что при повреждении лакокрасочного покрытия металл может начать подвергаться ржавлению.
Нанесение защитного покрытия из другого металла, который наделен большей устойчивостью к коррозии, и что немаловажно, не вступает в реакцию с основным металлом. Такой подход обеспечивает более надежную защиту, но, соответственно, и растет стоимость данного метода.
Это основные промышленные методы защиты, но существует множество других, которые применяются значительно реже, таких как термообработка, фосфатирование, ингибирование и изменение окружающей среды.
Что касается бытовых способов, то они в основном заключаются в использовании различных защитных покрытий. К ним могут относиться как лакокрасочные материалы, так и специализированные антикоррозийные средства. В этой области представлено просто огромное количество различных решений, о которых мы подробнее расскажем ниже. Существуют даже преобразователи ржавчины, которые предназначены для нанесения на уже поврежденные участки металлических изделий. Они могут частично восстановить поврежденные участки, однако степень восстановления зависит от глубины коррозии.

Во случае наличия определенного количества опасных веществ (АУ) в антикоррозийных составах, на упаковке обязательно будет знак, указывающий на опасность. С начала 2023 года в странах Европейского Союза продажа таких красок запрещена, равно как и их производство на экспорт с 2010 года.
Может ли вода защитить металл от коррозии?
На первый взгляд, это может показаться совершенно невозможным: как вода может защищать металл от ржавления? Сложно представить, чтобы такое вообще могло быть, поскольку это выглядит парадоксальным. Однако, научно-технический прогресс не стоит на месте и стремительно движется вперед, в том числе в области разработки новых видов лакокрасочных материалов.
Преимущества, которые обеспечивают лакокрасочные материалы (ЛКМ) на водной основе, способствуют ежегодному росту их производства и применения. На состоявшейся 3–4 декабря 2013 года в городе Дюссельдорф (Германия) конференции European Coatings Conference «Waterborne coatings» обсуждались достижения, проблемы и пути их решения в сфере водных лакокрасочных материалов.
Высокое качество систем двухкомпонентных (2К) полиуретанов на водной основе вкупе с низкой эмиссией растворителей ведет к высокому спросу на них в промышленности. Эти материалы успешно зарекомендовали себя в ряде сегментов рынка, поскольку они позволяют сбалансировать растущие требования к экологически чистым (или «зеленым») решениям с высокими стандартами качества, выдвигаемыми как промышленностью, так и профессиональными пользователями. Поставщики лакокрасочных материалов постоянно стремятся улучшать качество своих водных продуктов, а сырьевые компании работают над инновационными концепциями как для смол, так и для отвердителей.
В докладе, представленном д-ром Кристофом Ирлом (Christoph Irle) из Bayer Material Science (Германия), особое внимание было уделено производству и надежности этих составов. Данная проблематика будет способствовать развитию водных 2К систем, которые будут сопоставимы с самыми высокими стандартами, существующими для 2К полиуретанов на протяжении многих десятилетий. Тематику полиуретанов продолжил д-р Норберт Питшман (Norbert Pietschmann) из Института Lack und Fabric (Германия), выступив с докладом «Водные УФ-отверждаемые ЛКМ для защиты стали от коррозии». В этом ходе испытаний противокоррозионных свойств пигментов, ингибиторов, связующих веществ или их комбинаций использовались электрохимические измерения, позволяющие значительно ускорить получение результатов. Этот метод
позволяет определить оптимальную комбинацию связующего, состоящую из смеси УФ-отверждаемых и физически высыхающих дисперсий. Кроме того, был обнаружен подходящий и эффективный способ выбора антикоррозионных пигментов и ингибиторов. Исходя из предварительных исследований, можно создавать рецептуры с отличной адгезией и коррозионной стойкостью. После нанесения на сталь было проверено испарение влаги и УФ-отверждение, а также выполнены испытания на стойкость к соляным туманам и конденсации влаги. Электрохимические исследования подтвердили высокую адгезию и защитные свойства от коррозии, однако эти результаты были достигнуты только на стальных поверхностях, имеющих цинкфосфатный подслой.
Защита металла от коррозии в домашних условиях
Существуют ли «народные» средства для борьбы с ржавчиной?
Как обычное железо, так и высококачественная сталь, находясь в условиях влажного воздуха, характерного для гаражей, сараев и других вспомогательных помещений, подвергаются коррозии, постепенно покрываясь рыхлой буро-коричневой пленкой ржавчины. Часто совершенно новая вещь, оставленная на улице или «заброшенная» на даче зимой, покрывается нежелательной бурой коростой. Ржавчина, которая представляет собой смесь оксида железа Fe2O3 и метагидроксида железа FeO(OH), не защищает поверхность от дальнейшего воздействия кислорода и влаги. Со временем это приводит к полной деградации изделий из железа.
Существуют эффективные методы удаления ржавчины. Например, применяя разбавленные растворы соляной или серной кислот с добавлением ингибитора кислотной коррозии уротропина, можно гораздо легче очистить поверхность. Ингибиторы (от латинского «ингибео», что означает «останавливаю» или «сдерживаю») — это вещества, замедляющие химические реакции, в данном случае препятствующие распаду металла при взаимодействии с кислотой. Однако ингибиторы не мешают самой кислоте взаимодействовать с оксидами и гидроксидами железа, что и составляет основу ржавчины.
Если у вас ржавые оконные шпингалеты, мелкие детали велосипеда, болты или гайки, то их можно погрузить в 5% раствор кислоты с добавлением 0,5 г уротропина на литр. Для крупных предметов этот раствор наносится при помощи кисти.
Использование растворов сильных кислот без ингибиторов может принести больше вреда, чем пользы: можно растворить не только ржавчину, но и сам предмет, поскольку железо является активным металлом и вступает в реакцию с сильными кислотами, выделяя водород и образуя соли. В качестве ингибитора кислотной коррозии можно использовать и ботву картофеля. Для этого в стеклянной банке помещают свежие или сушеные картофельные листья и заливают их 5-7%-м раствором серной или соляной кислоты, следя за тем, чтобы уровень кислоты был выше примятой ботвы. После 15-20 минут перемешивания содержимого банки, кислота готова к использованию для обработки ржавых железных изделий.
Преобразователи ржавчины способны превратить её в прочное покрытие коричневого цвета. На загрязненные участки наносят 15-30%-й водный раствор ортофосфорной кислоты и дают высохнуть на воздухе. Для повышения эффективности можно использовать ортофосфорную кислоту с добавлением, например, 4 мл бутилового спирта или 15 г винной кислоты на 1 л раствора ортофосфорной кислоты. Ортофосфорная кислота преобразует компоненты ржавчины в ортофосфат железа FePO4, который образует защитную пленку на поверхности. В то же время винная кислота связывает часть производных железа, создавая тартратные комплексы.
Металлические поверхности, сильно пораженные ржавчиной, можно обработать:
- смесью, состоящей из 50 г молочной кислоты и 100 мл вазелинового масла. В этом случае кислота превращает метагидроксид железа из ржавчины в растворимую в вазелиновом масле соль — лактат железа. После очистки поверхность протирается тканью, смоченной вазелиновым маслом;
- раствором 5 г хлорида цинка и 0,5 г гидротартрата калия, разведенных в 100 мл воды. Хлорид цинка в водном растворе подвержен гидролизу и создает кислую среду, где метагидроксид железа растворяется, образуя растворимые комплексы железа с тартрат-ионами;
Чтобы отвинтить приржавевшие гайки, можно использовать керосин, скипидар или олеиновую кислоту для смачивания. Через некоторое время гайку удается снять. Затем можно поджечь керосин или скипидар, которыми мы смачивали гайку. Обычно это оказывается достаточным для разделения гайки и болта. Альтернативный способ заключается в том, чтобы прикладывать к гайке горячий паяльник. Затем металл гайки расширяется, и ржавчина отходит от резьбы. В этот момент в образовавшуюся щель между гайкой и болтом можно добавить несколько капель керосина, скипидара или олеиновой кислоты, и гайка легко отвернется ключом.
Коррозия вызывает немало проблем и в строительстве. Страдают металлические конструкции, например, гаражи, ангары, заборы, несущие элементы каркасных зданий, крыши. Этот «беспощадный враг» не щадит сантехнические системы и бытовые приборы, особенно те, что подвергаются действию воды.
Ознакомление с образцами тонколистового металла, проволоки и пластмасс
- Ознакомьтесь с образцами тонколистового металла, проволоки и искусственных материалов, предложенными учителем.
- Определите цвет образца и название металла или сплава.
- Измерьте толщину образца металла и проволоки.
- Проведите эксперимент: согните стальную и медную проволоку одинакового диаметра и сделайте выводы.
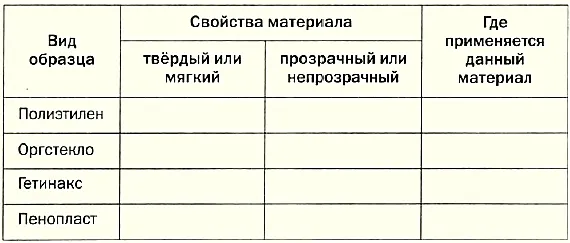
- Запишите результаты наблюдения в таблицу, отметьте, где применяется материал образцов.
- Проанализируйте предложенные образцы пластмасс (например, полиэтилен, органическое стекло, гетинакс, пенопласт). Запишите результаты исследования в таблицу.
Найдите в интернете информацию о других искусственных материалах, используемых человеком в научно-исследовательской деятельности, технике и повседневной жизни.