Представим еще один простой способ определить, какие из примесей в воде имеют больший объем — магний или кальций. Соли магния характеризуются меньшей растворимостью, что приводит к образованию осадка, и, кроме того, они обладают горьким привкусом.
Жесткая и мягкая вода — что это значит. Виды жесткости воды
Нередко клиенты интересуются у нас как у экспертов более детальной информацией о том, что такое жесткая и мягкая вода, какие у них существуют отличительные характеристики, а также как можно смягчить жесткость воды. Мы подготовили несколько статей, где описаны эти аспекты, и надеемся, что вы найдете исчерпывающие ответы на большинство своих вопросов относительно жесткости воды.
Объясняя простыми словами, жесткая вода представляет собой H2O, в составе которого содержится значительное количество растворённых солей щёлочноземельных металлов, преимущественно кальция и магния, то есть катионов Са и Mg. В свою очередь, мягкая вода — это такая вода, в которой концентрация этих солей существенно ниже. Чтобы измерить количество так называемых «солей жесткости» в воде, используют миллиграмм-эквиваленты на литр — мг-экв./л. Один мг-экв./л. подразумевает, что в литре воды содержится 20,04 мг катионов кальция или 12,16 мг катионов магния (что определяется путем деления атомной массы на валентность).
Существуют различные классификации жесткости воды. В России воду считают жесткой, если совокупная концентрация солей превышает 10 мг-экв./л. Воду, в которой содержится от 2 до 10 мг-экв./л. солей, определяют как средне жесткую, а вода с концентрацией солей менее 2 мг-экв./л. квалифицируется как мягкая.
Интересный факт: дождевая вода обычно характеризуется как мягкая, так как перед тем, как выпасть на землю в виде дождя, она испарялась. В процессе испарения «соли жесткости» не могут пройти в водяной пар, что приводит к естественной фильтрации. Жесткость же воды увеличивается, когда она проходит через почву и поглощает соли из почвы.
 |
 |
| Государственный стандартный образец (ГСО) «Общая жесткость воды» |
Набор для измерения жесткости воды |
Откуда взялись названия «жесткая» и «мягкая»
С незапамятных времен люди замечали, что вещи, выстиранные в одной воде, остаются мягкими после высыхания, тогда как при стирке в другой воде они становятся грубыми и жесткими. Поэтому логично, что воду, которая делает вещи мягкими, они стали называть мягкой, а ту, что делает их жесткими, — жесткой.
Интересно отметить, что иногда люди воспринимают мягкую воду как «живую», а жесткую, соответственно, как «мертвую». Это мнение в корне ошибочно. Да, существуют такие термины, как «живая» и «мертвая» вода, но они не имеют отношения к мифам о целебных свойствах живой воды и вредных качествах мертвой. Это скорее теория, которая не получила официального признания, но и не была опровергнута: считается, что вода с щелочной реакцией может обладать определёнными полезными свойствами, и именно она называется «живой». В то время как вода с кислотной реакцией, которую называют мертвой, не имеет таких свойств. Тем не менее, это понятийно никак не связано с жесткостью или мягкостью воды.
Зачастую клиенты обращаются к нам, чтобы получить более детальную информацию о жесткой и мягкой воде, их особенностях и методах смягчения. Мы подготовили несколько статей на эту тему и надеемся, что вы сможете найти в них ответы на большинство ваших вопросов.
В мире существуют различные методики оценки жесткости воды. Например, в России Госстандарт установил единицы измерения в моль на кубический метр. Число, представляющее жесткость в моль на кубический метр, соответствует значению жесткости в миллиграмм-эквивалентах на литр. Западные страны, в свою очередь, применяют степень жесткости, которая может быть выражена в немецких (d°, dH), французских (f°) и американских (ppm CaCO3) единицах.
Для создания комфортных условий для содержания аквариумных рыбок важно использовать воду с оптимальной жесткостью и определённым кислотно-щелочным балансом. Для увеличения жесткости воды применяются такие материалы, как известняк и мрамор. Существует прямая связь: чем мягче вода, тем быстрее она приобретет повышенную жесткость. Альтернативный метод — это химический подход, при котором используются хлористый кальций и магнезия. Наиболее эффективный результат достигается при совместном использовании обоих веществ.
Чтобы снизить жесткость воды, необходимо ее прокипятить. Сколько времени это нужно делать? Для сокращения жесткости вдвое, рекомендуется кипятить воду в течение как минимум получаса. Другой способ уменьшить жесткость — вымораживание. Для этого воду помещают в пластиковый контейнер и ставят в морозильную камеру. Замерзший лед затем растапливают, и полученную воду применяют в кулинарии или в любых других целях.
Если объем обрабатываемой воды велик, удобнее применять специальное оборудование. В последние годы во многих домах получили популярность установки обратного осмоса. Для расчета необходимого объема водопроводной воды можно использовать формулу: необходимо вычесть объем воды, поступающей из водопровода, из объема с заданной жесткостью, который требуется получить.
Часто методы умягчения комбинируют. Например, одну часть солей жесткости удаляют с помощью реагента, а другую — с использованием катионного обмена. Приведём уравнения содово-известкового метода умягчения:
Са(НСО3)2 + Са(ОН)2 = 2СаСО3 + 2Н2О
В результате Mg(OH)2 коагулирует и выпадает в осадок. Затем, для устранения некарбонатной жесткости, вводится Na2CO3. Следующие химические реакции выглядят следующим образом:
Na2CO3 + CaSO4 = CaCO3 + Na2SO4 и Na2CO3 + СаС12 = СаСО3 + 2NaCl.
В результате этих реакций образуется углекислый кальций, который затем также выпадает в осадок. Реагенты вводятся в разные зоны системы:
- хлор — в трубы всасывания;
- коагулянт — в трубопровод перед смесителем или прямо в смеситель;
- известь — вместе с коагулянтом;
- активированный уголь — перед фильтрами;
- хлор и аммиак — в фильтрованную воду.
К таким подходам, как опреснение, обессоливание, удаление растворённых газов и железа, а также стабилизация, применяются специальные методы очистки. Например, когда речь идет о снижении жесткости, используются методы катионирования или ионного обмена, согласно которым происходит обессоливание, и выходная вода не содержит ни анионов, ни катионов солей.
Как измерить жесткость
Чтобы оценить показатели жесткости воды, применяют различные методы:
- Комплексонометрическое титрование с использованием трилона Б. Этот метод считается сложным, но самым точным.
- Покупные тесты. Хотя они не обеспечивают 100% точности, их простота и доступность делают их популярными.
- Измерение электропроводности с использованием кондуктометра.
- Применение ионометра и ионо-селективных электродов.
- Метод титрования проб воды с использованием соляной кислоты. Этот подход является сложным и менее точным. Аналогично можно говорить о тестах с использованием хозяйственного мыла.
Под титрованием понимается добавление в воду реагента необходимой концентрации. Концентрация солей жесткости определяется на основе реакции реагента с водой. Приготовить реактив очень просто – достаточно смешать кислоту с дистиллированной водой в пропорциях, гарантирующих безопасное использование. Получившийся раствор не представляет угрозы.
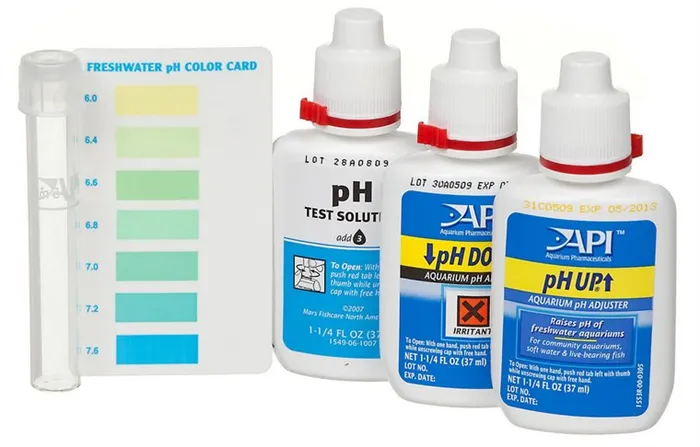
Самый простой способ — это использование готовых тестов. Для этого 5 мл воды помещают в стаканчик, а затем, по каплям, добавляют содержимое теста. Каждую каплю необходимо тщательно перемешивать. Так следует продолжать до тех пор, пока цвет жидкости не изменится на зеленый вместо розового.
Жесткая вода. Она может быть результатом как искусственного растворения примесей, так и естественного поступления влаги, проходящей через слои почвы, что в итоге приводит к высокой концентрации растворенных веществ. Наиболее распространенным примером жесткой воды является морская вода.
Шкала жесткости воды или как определить параметр по таблице
Прежде всего, представляем график, на основании которого любую жидкость можно разделить на различные классы:
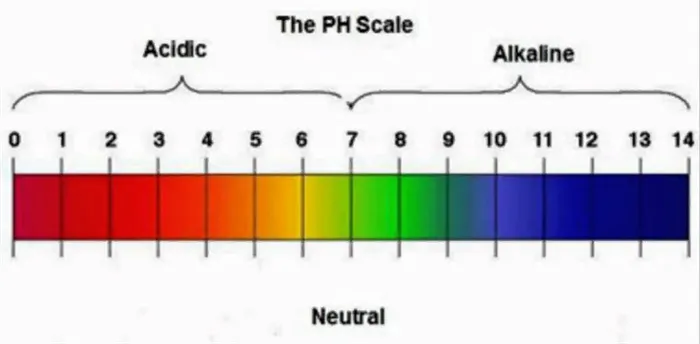
Alkaline – щелочная, она также известна как карбонатная. Степень её жесткости определяется наличием и концентрацией карбонатов и гидрокарбонатов кальция и магния. Особенность таких вод состоит в том, что указанные микроэлементы выпадают в осадок сразу после кипячения, поэтому такие растворы называются непостоянными или временными.
Вторая часть шкалы Acidic — это кислоты, содержащие соли, но не карбонаты и гидрокарбонаты, а кислотные соли на их основе. Эти соединения являются более устойчивыми.

1,5 м3/ч Для технической воды

1,5 м3/ч Для технической воды

Существует также понятие общей жесткости, которое фиксирует суммарное количество всех примесей. Как правило, в бытовых ситуациях акцент ставят именно на общую жесткость, определяя итоговую сумму микроэлементов. Однако в некоторых случаях важно обращать внимание на состояние магниевых и кальциевых солей, их соединений. Если вы столкнетесь с подобными шкалами в анализе жидкости или в иной ситуации, можете ориентироваться на цветовую градацию и диаграмму выше. То есть от 0 до 7 у вас будут кислотные соли, а с 7 до 14 — гидрокарбонаты.
Единицы измерения
Разобравшись, какую воду относят к жесткой, что определяет общую жесткость и какие виды существует, теперь стоит обсудить, в каких единицах измеряется этот показатель и какие факторы на него влияют.
К сожалению, в настоящее время нет единого мирового стандарта, поэтому, работая с оборудованием европейского производства, следует быть готовыми к обозначениям, которые могут показаться непонятными. Российские ученые установили следующие единицы: моль на кубический метр. Перед этой величиной указывается число, соответствующее количеству перевода в миллиграммы на литр. Можно встретить и другие обозначения:
d° или dH — были изобретены в Германии и применяются по всей территории Запада;
ppm CaCO3 — применяется в США.
Необходимо отметить, что в России выражение общей жесткости в моль/м3 начало использоваться лишь с 1952 года. До этого времени расчеты осуществлялись в градусах, которые соответствовали современным немецким градусам.
Когда каким-либо образом уже установлено, что вода обладает повышенной жесткостью, возникает логичный вопрос — возможно ли снизить ее жесткость в домашних условиях? Ответ будет положительным. Однако следует понимать, что это потребует приложить определенные усилия. Способ борьбы с жесткостью воды зависит от конкретных условий.
Если требуется справиться с жесткостью в небольшом объеме жидкости, можно использовать метод кипячения. Это не требует применения химических реагентов или сложной техники. Высокая температура способствует разложению проблемных веществ, которые оседают на дно. Кипяченую воду можно использовать для различных бытовых и технических нужд. Тем не менее, таким образом невозможно устранить все вещества, повышающие жесткость, а кроме того, появляется другая проблема — что делать с образовавшимся осадком или накипью.
К тому же, этот процесс занимает время и требует энергии или топлива. В некоторых случаях кипяченая вода может не подойти для определённых нужд. Кроме того, убрать лишнюю жесткость можно посредством метода отстаивания. Однако стоит отметить, что отстаивание занимает немалое время и подходит в основном для полива растений.
Отстаивание питьевой воды оправдано только в том случае, если ее жесткость слегка превышает норму. Метод вымораживания также может быть эффективным. При таком способе можно избавиться от неугодных солей без ухудшения качества воды, но получится в итоге совсем немного жидкости. Возможен и альтернативный подход с использованием пищевой и кальцинированной соды; отдельные аспекты данного метода полезны, но полученная таким образом вода не рекомендуется для питья.


Также извлекать полезные свойства из воды можно с помощью уксуса или лимонной кислоты. Эти средства могут помочь немного уменьшить жесткость, но одновременно могут повысить кислотность. Следовательно, для питьевого использования такие способы не подходят, однако они могут быть рекомендованы для косметических процедур.
Для решения проблемы с накипью в стиральных и посудомоечных машинах можно воспользоваться обычной поваренной солью или специальной солью, рекомендованной производителем бытовой техники. Но наиболее универсальным методом, особенно при водоснабжении из колодца или скважины, является установка фильтров. Их также можно использовать для очистки водопроводной воды. Структура и принцип действия фильтра не критичны, куда важнее — их производительность.
Фильтры-кувшины работают на объем от 1 до 3 литров чистой жидкости. Это вполне достаточно для приготовления чая, кофе, нескольких порций супа или каши, а вот для больших объёмов приготовление может стать невозможным. Более эффективными являются ионообменные фильтры. Однако они не предназначены для получения питьевой воды и должны подключаться к системам канализации.
В случае с магнитными и электромагнитными умягчителями, а также мембранными фильтрами решить проблему получения питьевой воды не удастся. Последние могут помочь при дополнительной контролируемой реминерализации, но этот процесс является дорогостоящим и сложным.