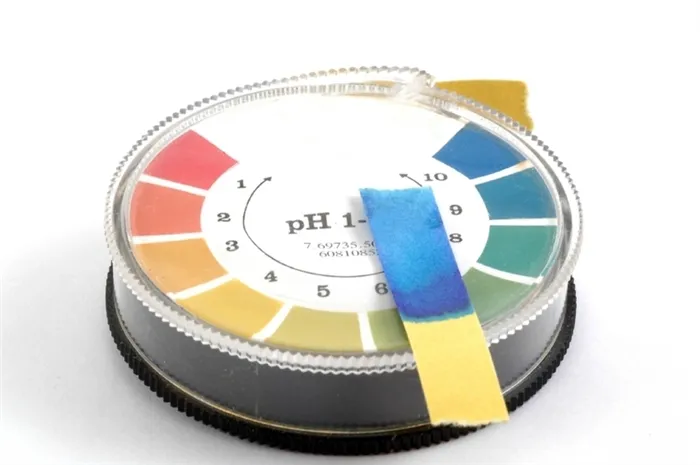
Диапазон значений pH для различных растворов формируется на основе стабильности ионного продукта воды. Число «7» в этом диапазоне соответствует нейтральному состоянию. Значения pH, расположенные слева от 7, указывают на кислую среду, тогда как те, что расположены справа, показывают щелочную (или основную) среду.
Что такое pH воды
Уровень активности водородных ионов в воде является критически важным показателем, влияющим на оценку качества этой жидкости. Этот параметр определяет кислотно-щелочной баланс и влияет на множество биохимических процессов, происходящих в организме после употребления воды. В этом контексте мы детально рассмотрим, что такое pH воды, какие методы используются для его определения, а также способы, позволяющие изменить уровень pH.
В данном материале вы сможете узнать:
Чем может быть опасен низкий уровень pH воды?
С учётом быстрого темпа жизни в современном обществе, а также влияния неправильного питания и вредных пищевых привычек, уровень pH в организме человека часто оказывается понижен. Это приводит к смещению уровня pH в сторону более кислой среды. Более низкие значения pH свидетельствуют о кислой реакции, в то время как значение pH 7 указывает на нейтральную среду, а 14 — на щелочную. Подобная ситуация может вызвать серьезные проблемы со здоровьем. Решением может стать регулярное употребление минеральной воды с оптимальным уровнем активности водородных ионов. Поэтому следует внимательнее отнестись к значению pH той воды, которую вы пьёте ежедневно.

Какой же уровень pH должен быть у воды? Специалисты утверждают, что это значение должно находиться в пределах, примерно соответствующих нормальному pH крови человека, который составляет около 7,5. Поэтому питьевая вода считается оптимальной в диапазоне от 7 до 7,5. Чистая питьевая вода с нормальным уровнем pH благоприятно влияет на обмен веществ, способствует увеличению продолжительности жизни и оптимизирует процесс кислородного обмена. В отличие от этого, сладкие, газированные и цветные напитки могут понижать уровень pH крови человека. Это снижение часто сопровождается неприятным ощущением сухости в полости рта.
Поэтому нужно отдавать предпочтение воде с «правильным» значением pH. Эта информация легко доступна на этикетках бутылок. Необходимо отметить, что фильтры с наполнителями и абсорбентами не могут в полной мере заменить настоящую природную воду с оптимальным значением pH. Некоторые люди пытаются изменить уровень pH воды, добавляя в неё сок лимона или огурца, однако не всегда такой подход дает желаемые результаты. Альтернативный популярный метод изменения pH воды — это электролиз. В результате этого процесса получают щелочную и кислую воду в двух емкостях: щелочная вода с высоким уровнем pH считается «живой» и используется для различных лечебных целей, тогда как кислая вода рассматривается как «мертвая» и, как правило, применяется для умывания лица.
Однако указанные методы не всегда подходят для ежедневного использования. В этой ситуации остаётся единственный эффективный подход — выбирать природную воду с низким содержанием минералов и подходящим для здоровья уровнем кислотности.
Измерение pH воды
Важно помнить, что человеческое тело на 70% состоит из воды. Продукты метаболизма клеток имеют кислую реакцию, но большинство жидкостей в организме, за исключением желудочной кислоты, имеют слегка щелочную природу. Особенно критично следить за уровнем pH в крови. Организм функционирует должным образом только тогда, когда кровь имеет слегка щелочной уровень pH, равный 7,35-7,45.
При попадании большого количества кислоты в кровь и межклеточную жидкость может произойти нарушение кислотно-щелочного баланса. Даже малейшее отклонение от указанных значений pH (7,35-7,45) может вызвать серьезные проблемы со здоровьем. Если кислотность крови продолжает повышаться, и уровень pH остается ниже 6,95, может случиться кома, что создаёт реальную опасность для жизни. Исходя из этого, контроль уровня pH питьевой воды становится крайне важным, так как это один из основополагающих показателей её качества.
Вы можете самостоятельно измерить pH воды в домашних условиях. В качестве простого pH-метра можно использовать маслостойкую индикаторную бумагу, которая изменяет цвет при краткосрочном погружении в исследуемую жидкость. Примером может служить использование индикатора в воде из озера: она станет красной в кислой среде и синей в щелочной. После этого следует сопоставить цвет с цветовой шкалой, где каждый оттенок соответствует определенному уровню pH. Данный метод измерения pH является самым простым и экономически доступным.
Для более точного определения уровня pH в воде применяются рН-метры. Эти устройства стоят дороже, чем индикаторная бумага, но обеспечивают более высокую точность измерений.
Измерители pH воды бывают бытовыми (портативными) и лабораторными. Первый вариант чаще используется в быту. Рассмотрим их подробнее. Они различаются по следующим характеристикам:
Наличие автоматической калибровки или её отсутствие.
Если калибровка выполняется, это определяется числом калиброванных точек (одна или две). Эти точки — буферные растворы, которые служат для калибровки pH-метра, и рекомендуется приобретать приборы с автоматической калибровкой для повышения точности.
Существуют специализированные тест-полоски для определения уровня pH. Эти полоски просты в использовании и имеют шкалу, позволяющую оценить концентрацию ионов водорода в жидкости. Однако такие контрольные средства могут быть дорогостоящими и не всегда доступны.
Несмотря на свои достоинства, водные pH-метры также могут иметь относительно высокую стоимость.
Для измерения pH воды возможно также использование самодельных тест-полосок.
Существует множество веществ, цвет которых изменяется в зависимости от уровня водородных ионов в жидкости. Например, если ввести ломтик лимона в чай, он приобретает желтый цвет вместо привычного коричневого.
Другие продукты, как вишневый сок или сок из изюма, также способны менять окраску в зависимости от кислотности. В природе представлено множество подобных органических индикаторов. На основе их свойств создаются самодельные тест-полоски, позволяющие определять уровень pH воды.
Еще одним примером служат вещества, содержащиеся в красной капусте. Этот овощ обладает пигментом антоцианом, который относится к флавоноидам и определяет цвет капустного сока, изменяющий цвет в зависимости от уровня кислотности.
При повышении температуры увеличивается распад слабых электролитов, включая воду. Это ведет к увеличению равновесной концентрации ионов и росту величины ионных продуктов. Соответственно, изменяется также водородный показатель нейтральной среды.
Нужен ли мне pH-метр?
В традиционных подходах к точному определению значения pH обычно применяется pH-метр. Из-за низкой точности субъективного определения цвета или визуальных маркеров, использование последних для получения точных значений часто нецелесообразно. Однако главными преимуществами индикаторов являются их доступность по цене, наглядность анализа и быстрота выполнения измерений.
Существует множество различных характеристик, которые определяют качество pH-метров. К их числу относятся: диапазон измерения pH (обычно от 0,00 до 14,00), рабочая температура, значение шкалы для определения (0,1 pH), а также точность (0,1 pH). Цены на эти устройства могут колебаться в пределах от 15 до 100 долларов США.
Для целей, таких как изготовление мыла и кремов, зачастую достаточно простейших моделей. Как правило, они обладают следующими характеристиками: диапазон измерения pH от 0,00 до 14,00, рабочая температура от 0 до 50°C, значение шкалы 0,1 pH и точность 0,1 pH. Гистограмма должна подвергаться регулярной калибровке.
Если pH-метр некорректно откалиброван и показывает неправильные значения, его необходимо откалибровать. Например, процесс калибровки можно выполнить с помощью аппарата типа pH 009. При этом калибровка других моделей осуществляется аналогичным образом.
Что же вам потребуется для калибровки? Прежде всего, это сам pH-метр, отвертка с насечками (часто входит в комплект), калибровочная жидкость и аккуратная рука. Если нужные инструменты отсутствуют, стоит позаботиться о необходимом запасе. Для калибровки pH-метра Budget 009 будет вполне достаточно раствора с pH 4,00 или 6,8, используемого в одной точке. Раствор должен быть при комнатной температуре. Если он хранился в холодильнике, перед применением его нужно достать и хорошо встряхнуть.
Теперь нужно окунуть pH-метр в калибровочный раствор. После этого необходимо подождать. На задней стороне прибора имеется регулировочный винт, который нужно поворачивать по часовой стрелке или против часовой стрелки в зависимости от показаний дисплея. Значение на экране должно совпадать с pH раствора. Таким образом проходит весь процесс калибровки!
Как пользоваться pH-метром
К каждому устройству обычно прилагается инструкция по эксплуатации.
Ниже приведена пошаговая процедура для небольшого pH-метра pH-PAL:
- Снимите защитную оболочку с нижней части устройства.
- Включите прибор, переместив верхний переключатель вправо.
- Погрузите прибор в тестируемую жидкость до появления отметки на кнопке.
- Энергично перемешивайте в течение 5-6 секунд. После стабилизации считайте показания индикатора.
- Если электрод оказывается сухим, подождите немного дольше для его термоформирования.
- Тщательно промывайте электрод дистиллированной водой после каждого измерения.
- Не забудьте выключить устройство и вернуть защитную крышку после каждого использования.
Нормы pH.
Растворы и жидкости можно оценивать по их кислотности.
Кислотность мочи.
Если рН мочи колеблется между 6,0 и 6,4 в утренние часы и между 6,4 и 7,0 вечером, значит, организм функционирует в норме. Оптимальный уровень pH мочи должен быть слегка кислым, в диапазоне между 6,4 и 6,5. Показатель pH мочи ниже 5,0 свидетельствует о высокой кислотности, в то время как уровень pH выше 7,5 указывает на высокую щелочность.
Реакция мочи важна для определения вероятности образования камней: уратные камни формируются в кислой среде, оксалатные камни появляются в нейтральной и слегка кислой среде, а фосфатные камни — в более щелочной. Например, если pH мочи превышает 5,5, шансы на образование камней мочевой кислоты крайне маловероятны, в то время как фосфатные камни не образуются, когда моча остается нещелочной. Лучше всего проверять pH мочи за час до приема пищи или через два часа после него.
Рекомендуется проверять уровень pH мочи два раза в неделю и два-три раза в день для более точного мониторинга.
С использованием лакмусовой бумаги с pH-индикатором можно быстро и просто контролировать реакцию мочи на изменения в рационе питания, принятие медикаментов или использование пищевых добавок. Улучшение уровня pH служит ярким показателем корректности подобранной диеты или лечения.
Кислотность мочи довольно изменчива в зависимости от употребляемых продуктов. Растительная диета способствует повышению щелочной реакции мочи, тогда как преобладание белковых продуктов, включая мясо, ведет к повышению кислотности мочи.
Факторы, такие как интенсивные физические нагрузки, также могут повышать кислотность мочи.
Увеличение кислотности мочи может быть связано с повышением кислотности желудочной среды. Однако снижение уровня кислотности желудочного сока не влияет на качество мочи.
Кислотность мочи становится индикатором многих заболеваний и состояний, а потому диагностика кислотности мочи имеет значительное диагностическое значение.
Кислотность слюны:
Уровень кислотности слюны зависит от скорости её секреции. В норме значение pH смешанной слюны человека колеблется от 6,8 до 7,4, однако может достигать 7,8 при быстром потоке слюны. В частности, уровень pH слюны, вырабатываемой околоушной железой, составляет 5,81, а в подчелюстной составляет 6,39. У детей средний уровень pH смешанной слюны равен 7,32.
Лучше всего определять уровень pH слюны между 10:00 и 12:00, а проводить измерения следует натощак, за два часа до или после еды. Стоит учитывать, что слюноотделение уменьшается в вечерние часы и ночью.
Для увеличения выделения слюны и, соответственно, повышения уровня pH, можно положить на тарелку ломтик лимона. Это визуально привлекательное представление пищи, оформленной зеленью и овощами, также будет способствовать выработке слюны. Это создает необходимые условия для подготовки организма к пищеварению, и в данном контексте процесс выделения желудочных соков становится ментальной стадией пищеварительной секреции.
Такие заболевания, как гастроэзофагеальная рефлюксная болезнь и фарингеальная рефлюксная болезнь, проявляющиеся в полости рта, могут оказывать существенное влияние на патологические процессы в ротовой полости. В результате попадания соляной кислоты уровень pH смешанной слюны может снизиться до уровня менее 7,0. При низких значениях pH слюна становится более щелочной, особенно в диапазоне 6,2-6,0, что ведет к локальной деминерализации зубной эмали, появлению эрозий в твердых тканях зубов и образованию кариозных полостей. Увеличивается количество слизи в слизистых оболочках, десна становятся воспаленными и опухшими.